Descubriendo
las células progenitoras
Disponer en el laboratorio de células capaces de diferenciarse
–o sea formar los diferentes tejidos del organismo– fue un
problema que ha desvelado a los científicos durante años.
Finalmente, en 1998, los investigadores norteamericanos James Thomson
y John Gearhart anunciaron que podían hacer crecer en el laboratorio
células troncales –o progenitoras– de origen humano.
Se abrió así la puerta al diseño de nuevas terapias
médicas que podrían curar varias enfermedades y contribuir
a una mayor eficacia en el trasplante de órganos.
Por Sergio Vianello.
Departamento de Biología Celular, Histología, Embriología
y Genética, FAcultad de MEdicina, UBA.
La célula huevo –o cigoto–, producto del asombroso
proceso de fecundación, es totipotencial, o sea que es capaz de
generar por sí misma un individuo. Cuando el cigoto llega al estadio
bicelular –es decir que se duplicó una vez–, cada una
de estas células puede potencialmente formar un feto. Recordemos
que los gemelos genéticamente idénticos se forman cuando
dos células totipotentes se separan y a partir de cada una de ellas
se desarrolla un individuo. Aproximadamente cuatro días después
de la fecundación, las células, que se han dividido por
mitosis, produjeron un aumento del número de células y una
reducción de su tamaño, ya que el volumen total del embrión
sigue siendo el del cigoto. Estas células se denominan blastómeras,
y comienzan a especializarse. Cuando el embrión está formado
por aproximadamente 16 células se llega al estadio de mórula
(Fig. 1). A partir de esta etapa, las células que constituyan el
macizo celular interno darán origen al embrión propiamente
dicho, mientras que la capa celular circundante contribuirá a la
formación de la placenta (Fig. 1).

Ampliar
Fecundación y embriogénesis.
Las blastómeras del macizo celular interno poseen la capacidad
de generar todos y cada uno de los tejidos y órganos del individuo
en formación –o sea que son células troncales o progenitoras–,
pero no pueden formar todos los tipos celulares necesarios para el desarrollo
fetal, como la placenta. Como su potencial no es total, es decir no son
totipotentes, las denominamos pluripotentes. A medida que estas células
pluripotentes se van dividiendo y diferenciando van perdiendo potencialidad
evolutiva, esto es, la capacidad de originar muchos tejidos diferentes;
cuando alcanzan el máximo grado de diferenciación quedan
circunscriptas a formar un único tipo celular. Por ejemplo, en
la tercera semana del desarrollo embrionario humano ocurre el proceso
de gastrulación, durante el cual se forman las tres capas germinativas
–el endodermo, el mesodermo y el ectodermo–. A partir de ese
momento, y siempre en condiciones normales, las células endodérmicas
sólo formarán tejidos de ese origen, ya que no tienen la
potencialidad de producir tejidos mesodérmicos o ectodérmicos.
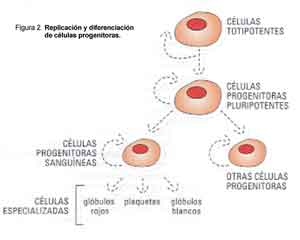
Estas células progenitoras más especializadas son denominadas
multipotentes. Un ejemplo clásico de células multipotentes
son aquellas que se ubican en la médula ósea y que dan origen
a los glóbulos rojos, los glóbulos blancos y las plaquetas;
son las células progenitoras sanguíneas (Fig. 2).
Ampliar
Al finalizar el desarrollo embrionario algunas células conservan
potencialidad evolutiva, forman parte del tejido al cual pueden dar origen
y son multipotentes. Se las denomina células troncales –o
progenitoras– de tejidos adultos, para diferenciarlas de las que
se encuentran en tejidos embrionarios. Estas células se han descripto
tanto en niños como en adultos.
Hasta hace poco se consideraba que las células progenitoras presentes
en tejidos específicos de adultos -tales como las sanguíneas
o las neurales-, estaban restringidas a dicho tejido. Este paradigma está
siendo revisado, ya que existen importantes evidencias que muestran que
células progenitoras de adultos obtenidas de un tejido pueden contribuir
a formar un tipo celular diferente cuando son expuestas a factores ambientales
apropiados.
Se sabe que las células progenitoras embrionarias tienen mayor
potencial para dividirse y diferenciarse que las células progenitoras
de adultos. Sin embargo, las células embrionarias presentan dos
inconvenientes fundamentales para ser útiles en medicina: por un
lado, deben obtenerse de embriones humanos, lo que genera importantes
conflictos éticos y, por el otro, estas células tienden
a diferenciarse espontáneamente en todos los tipos de tejido, lo
que hace necesario aprender cómo hacer para que se diferencien
sólo en el tipo celular deseado.
Las células progenitoras de la mayoría de los tejidos de
los mamíferos se replican -es decir que aumentan su número-,
y se diferencian por mecanismos asimétricos: cada célula
progenitora origina otra célula progenitora y una célula
hija diferenciada. Esta asimetría ocurre a nivel poblacional, no
individual, y facilita la respuesta ante cambios fisiológicos,
como por ejemplo, la necesidad de mayor producción de glóbulos
rojos después de una hemorragia, o de células de la piel
luego de quemaduras graves. Durante la división asimétrica
las células hijas adquieren diferentes potenciales de desarrollo
por la segregación desigual de factores citoplasmáticos
o por influencias diferenciales del medio. Los denominados factores de
transcripción -proteínas que interactúan con el ADN
presente en los cromosomas de la célula- regulan las divisiones
asimétricas de las células progenitoras. Cada linaje es
controlado por una combinación única de factores de transcripción.
Se sabe que existe una compleja interrelación de señales
entre las células progenitoras, sus hijas en diferenciación,
células vecinas y el nicho o micro ambiente en el que se encuentran;
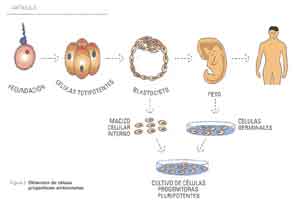
desde 1998 puede hacerse crecer en el laboratorio células progenitoras
de origen humano. Para realizar estos cultivos las células se obtienen
a partir del macizo celular interno de embriones humanos, o de células
tomadas de la región destinada a formar gónadas en fetos
nonatos (Fig. 3).
Ampliar
Existen múltiples razones por las que es importante poder aislar
y cultivar in vitro células progenitoras pluripotentes humanas.
Estas podrían ayudar a entender los complejos eventos que ocurren
durante el desarrollo humano, ya que se sabe que la activación
o la inactivación de determinados genes es crucial en este proceso,
pero no se conoce casi nada acerca de cuáles son los mecanismos
implicados. También el uso de células progenitoras puede
cambiar la forma en que se prueban las nuevas drogas farmacológicas,
ya que ellas permitirían establecer si el producto en ensayo produce
efectos teratogénicos -es decir, si se induce el desarrollo de
malformaciones- o no.
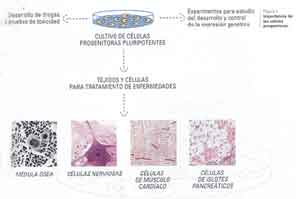
Pero quizás la aplicación más importante de las células
progenitoras pluripotentes es la posibilidad de generar células
y tejidos para ser empleados en terapia celular. En la actualidad se está
trabajando profusamente en el tema. Se citan a continuación algunos
ejemplos como muestra de lo revolucionario de estos avances (Fig. 4).
Ampliar
• Se podría inducir tolerancia específica de largo
plazo a órganos trasplantados. En este caso se haría un
trasplante simultáneo del órgano y de células progenitoras
sanguíneas del mismo donante, las cuales generarían células
inmunes que, por tener los mismos antígenos de histocompatibilidad
que el órgano trasplantado, diluirían la respuesta de rechazo
de las células inmunes del paciente.
• Para evitar el rechazo que se produce debido a la reactividad
de las células inmunes del paciente, se deben administrar altas
dosis de drogas inmunosupresoras, luego de un trasplante hepático.
Si se lograra repoblar el órgano trasplantado con células
progenitoras del paciente que lo recibe, se disminuiría considerablemente
la probabilidad de rechazo.
• La identificación de células progenitoras multi
y pluripotentes de islotes pancreáticos -donde se produce, entre
otras hormonas, la insulina- está en una fase temprana de desarrollo.
El trasplante de páncreas es muy dificultoso, y el de islotes aislados
requiere un muy alto número de células viables. Además,
las células de los islotes son difíciles de cultivar in
vitro, por lo que sería razonable realizar esfuerzos para encontrar
las condiciones experimentales en las cuales los islotes sean continuamente
generados a partir de células progenitoras.
• Diversos estudios realizados en ratones demostraron que células
musculares cardíacas -preparadas a partir de células progenitoras
pluripotentes- repoblaron el corazón y trabajaron junto con las
células del huésped. Es posible entonces suponer que el
trasplante a pacientes con insuficiencia cardíaca crónica
de células de músculo cardíaco generadas a partir
de células progenitoras podría mejorar el funcionamiento
del corazón.
• En una publicación de enero de 2002 se muestra que es factible
que células progenitoras embrionarias de ratón se diferencien
en neuronas que son luego trasplantadas en el cerebro de ratas. Es decir
que el trasplante de células progenitoras multipotentes o células
progenitoras de adultos de sistema nervioso central podría servir
para tratar enfermedades neurodegenerativas como el Parkinson y el mal
de Alzheimer.
Otro avance científico revolucionario es lo que se ha dado en llamar
clonación o transferencia nuclear somática. Esta técnica
consiste en fusionar el núcleo de una célula somática
-cualquier célula del organismo, excepto las gametas- con un ovocito
-u óvulo- no fertilizado, al que previamente se le extrajo su propio
núcleo. Luego esta célula ‘artificial’ es estimulada
para que se divida, originando así células totipotentes
que, implantadas en un útero, pueden desarrollar un individuo genéticamente
idéntico al que donó el núcleo.
Combinando esta técnica con los avances alcanzados con las células
progenitoras podría utilizarse una célula somática
de un paciente que padezca alguna de las enfermedades que pueden ser tratadas
con terapia celular y transferir el núcleo como se explicó
en el párrafo anterior. Cuando la célula, luego de ser estimulada,
llegue al estadio de blastocisto se podría extraer el macizo celular
interno donde se encuentran las células progenitoras embrionarias
que se utilizarán para la terapia (Fig. 5).

Ampliar
Estas células, genéticamente iguales a las del paciente,
no provocarían rechazo ya que no serían reconocidas como
ajenas por el organismo, y por lo tanto no habría que tratar al
paciente con drogas inmunosupresoras que suelen tener importantes efectos
tóxicos.
La clonación de embriones humanos como fuente de células
es tema de debate en varios sectores de la sociedad, ya que estos embriones
son personas en potencia. El británico lan Wilmut, creador de la
oveja Dolly, el primer mamífero clonado a partir de células
adultas, sostiene que el punto de vista de aquellos que consideran la
vida sagrada desde la concepción debe respetarse. En contraposición
están aquellos que, como él, consideran al embrión
como un conjunto de células insensibles, hasta que llegan a un
desarrollo más avanzado. En el año 2000, en Gran Bretaña,
se legisló a favor de la clonación terapéutica, pero
la idea de la clonación humana con fines reproductivos creció
en paralelo y generó un rechazo casi unánime. En otros países,
tales como los Estados Unidos, el Estado no puede otorgar fondos para
investigaciones con embriones humanos, pero no se prohíben los
experimentos que se realicen utilizando dineros privados.
Los trabajos con células progenitoras y los resultados obtenidos
hasta el presente generan una enorme expectativa sobre los alcances de
estas técnicas y se multiplican las dudas y preguntas que aún
no tienen respuesta: ¿se podrán curar realmente enfermedades
para las que por ahora no hay solución?, ¿será posible
contar con una fuente de células capaces de diferenciarse en el
tipo celular requerido?, ¿los trasplantes de órganos pasarán
a ser un tratamiento de rutina en los hospitales?, ¿cuáles
serán las consecuencias evolutivas de la aplicación de estas
nuevas técnicas? La lista de preguntas puede continuar, pero la
respuesta a todos estos interrogantes se irá revelando con el paso
del tiempo y el a veces lento pero efectivo avance de la ciencia.
 Sergio
Vianello: Licenciado en Ciencias Biológicas de la Facultad de Ciencias
Exactas y Naturales (UBA). Jefe de Trabajos Prácticos en la Unidad
del Departamento de Biología Celular, Histología, Embriología
y Genética de la Facultad de Medicina (UBA). vianello@mail.retina.ar Sergio
Vianello: Licenciado en Ciencias Biológicas de la Facultad de Ciencias
Exactas y Naturales (UBA). Jefe de Trabajos Prácticos en la Unidad
del Departamento de Biología Celular, Histología, Embriología
y Genética de la Facultad de Medicina (UBA). vianello@mail.retina.ar
|